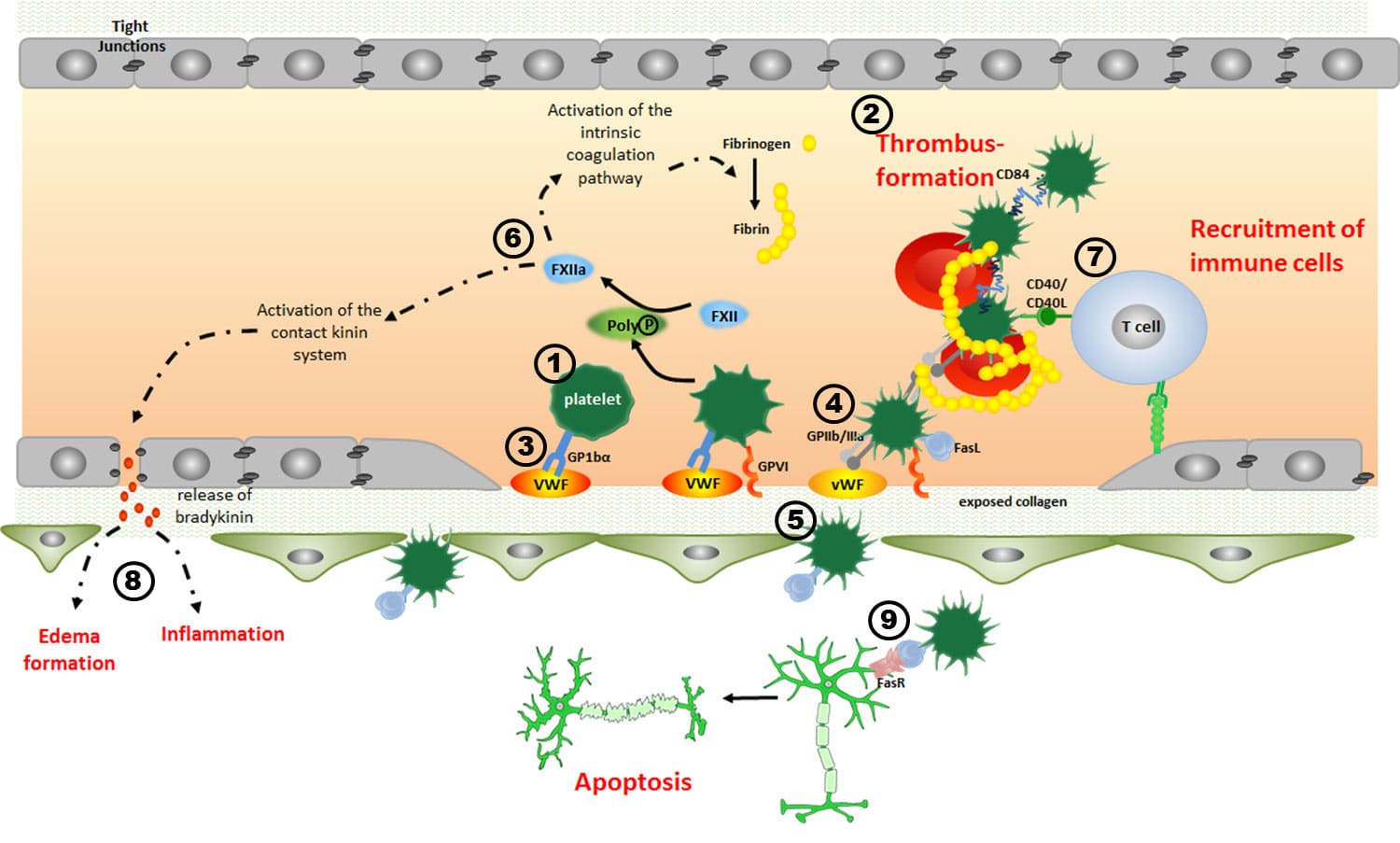
In den letzten Jahren haben unsere Arbeitsgruppen die pathophysiologische Rolle der Blutplättchen (1) als Mediatoren der Thrombusbildung (2) während der akuten Phase des ischämischen Schlaganfalls umfassend charakterisiert. Wir konnten zum Beispiel zeigen, dass die Inhibierung der Thrombozytenadhäsion durch die Blockade des Plättchenrezeptors Glykoprotein (GP) – Ib (3) eine mikrovaskuläre Thrombose im ischämischen Mäusehirn verhindert, ohne das Risiko einer intrakraniellen Blutung zu erhöhen. Überraschenderweise schützt eine Blockade des GPIIb / IIIa (4), ein wichtiger Rezeptor für die finale Thrombozytenaggregation, nicht vor einem akuten experimentellen Schlaganfall, sondern verursacht einen massiven Anstieg intrakranieller Blutungen (5). Dies deutet darauf hin, dass nach einem Schlaganfall neben Thrombosen auch andere pathophysiologische Mechanismen existieren und sekundäre Hirnschäden verursachen können. Hier ist die Inflammation hervorzuheben, da Thrombenbildung und Inflammation beim akuten ischämischen Schlaganfall eng miteinander verwoben sind („Thrombo-Inflammation“). Beispielsweise interagieren Blutplättchen nach einem Schlaganfall in der zerebralen Vaskulatur mit Endothelzellen (6) und T-Zellen (7), und fördern so sekundäre Gewebeschädigungen und kapillare Verschlüsse (8). Da die Mehrheit der Schlaganfallpatienten nicht für Akuttherapien wie die Rekanalisierung in Frage kommt, zielen aktuelle therapeutische Bemühungen darauf ab, die Geweberegeneration in fortgeschrittenen Stadien zu fördern. Hier ist die Rolle der Thrombozyten noch gänzlich unbekannt. Eine Plättchenaktivierung im ZNS wurde bereits mit gänzlich unerwarteten Krankheitsbildern assoziiert, z.B. in Autoimmunerkrankungen wie die Multiple Sklerose, bei der Thrombozyten Organschäden durch Leukozytenrekrutierung und Mikrogliaaktivierung beschleunigen. Blutplättchen können auch die Gewebehomöostase außerhalb des Blutgefäßsystems beeinflussen. Diese Fähigkeit war bis vor kurzen noch völlig unbekannt; z.B. können Thrombozyten Apoptose induzieren (9), ein wichtiger Prozess während der Reorganisation und Remodellierung von Geweben. So konnten wir in Modellen des akuten ischämischen Schlaganfalls und der Netzhautdegeneration zeigen, dass Thrombozyten mit nicht-leukozytären apoptotischen Zellen assoziiert sind.
Die zentrale Hypothese dieses Projekts ist daher, dass Thrombozyten eine zentrale Rolle bei der Remodellierung und Reparatur des Hirngewebes während der Rehabilitationsphase (Spätphase) eines ischämischen Insults spielen. Zusammenfassend wollen wir analysieren, was für Effekte eine Veränderung der Thrombozytenfunktion und -aktivierung auf die sekundäre Thrombusbildung, Gewebinflammation und Rehabilitation hat. Darüber hinaus werden wir die Rolle von Blutplättchen außerhalb des Gefäßsystems charakterisieren – insbesondere ihr Potential Apoptose, Angiogenese und neuronale Plastizität zu modulieren.